
En tant que filiale d’International Drug Development (IDD), BVP renforce les capacités du groupe en ajoutant une plateforme dédiée à l’exploitation et à la commercialisation pharmaceutique, venant compléter l’expertise reconnue d’IDD en développement et en consulting réglementaire.
Ensemble, le groupe propose une solution intégrée et fluide pour accompagner la mise sur le marché de vos produits.
Basée à Paris, BVP est une société européenne dirigée par une équipe de professionnels expérimentés, cumulant plus de 30 ans d’expertise dans l’industrie pharmaceutique.
Communiqué de presse du 6 janvier 2026


Le site web repensé reflète l’engagement d’IDD à fournir des solutions haut de gamme et sur mesure sur l’ensemble de la chaîne de valeur du médicament. Les principales caractéristiques du nouveau site incluent :
- Descriptifs détaillés des services : Un aperçu clair des services principaux d’IDD, y compris l’accompagnement pré-autorisation des actifs, le suivi post-autorisation des médicaments et les services de plateforme commerciale.
- Navigation simplifiée : Une conception intuitive qui permet aux visiteurs de trouver facilement les informations dont ils ont besoin.
- Un design moderne et responsive : Une expérience fluide sur tous les appareils.
« Nous sommes ravis de lancer notre nouveau site web et d’offrir à nos clients et partenaires une expérience en ligne plus engageante et informative ».
« Ce nouveau site témoigne de notre engagement constant envers l’excellence et l’innovation dans le secteur du conseil pharmaceutique. »
Le nouveau site web sera régulièrement mis à jour avec des actualités, des analyses et des informations sur l’entreprise. Les visiteurs sont invités à explorer le site et à en apprendre davantage sur les services d’IDD
Tout d’abord, Clarisse Ribeiro, arrivée en [DATE], diplômée de [DIPLOME], spécialiste en [MISSIONS IDD]
Ensuite, Mohamed ALILI, docteur en pharmacie depuis 2020 en Algérie, réalise un stage en vue de faire reconnaître son diplôme en France. Il s’occupe de l’Assurance qualité et des Affaires réglementaires sous la responsabilité directe d’Anne Walter.
Enfin, nous avons accueilli un second stagiaire en mai 2025. Swann Walch réalise son stage de cinquième année de pharmacie sous la responsabilité de Stéphane Simon et participe au business development ainsi qu’à l’intégration de l’IA dans les procédures de l’entreprise.
Ces recrutements témoignent du dynamisme de nos structures, de leur attractivité auprès des jeunes talents, et de notre engagement à faire vivre des valeurs d’excellence, de transmission et d’innovation.
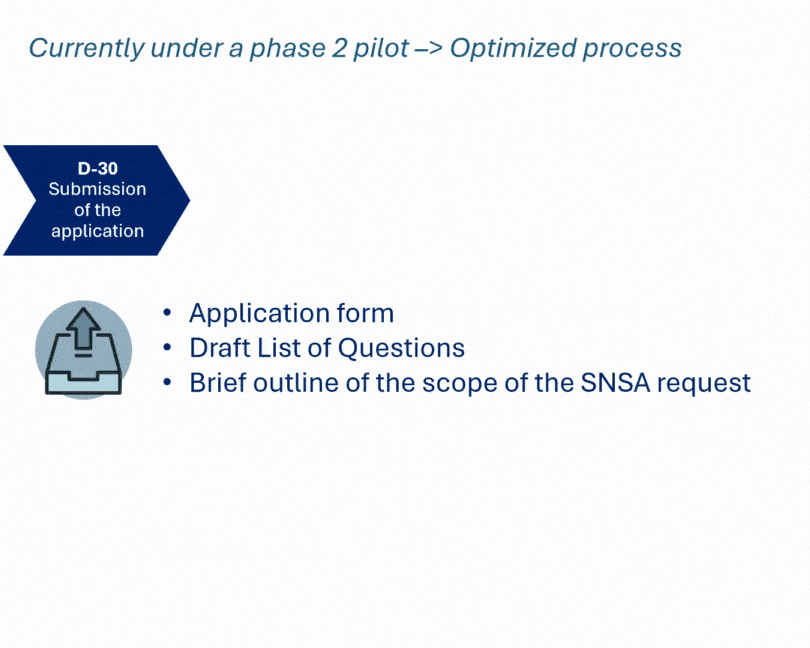
Cette démarche coordonnée a permis d’aborder de manière structurée les aspects CMC, non cliniques et cliniques, là où les guidelines étaient peu précises. Résultat : une vision plus claire et sécurisée du plan de développement, en cohérence avec les attentes des autorités.
🔗 En savoir plus sur le SNSA
– Anne Walter



Présents à la conférence RAPS Euro Convergence 2024 à Bruxelles, nous avons échangé autour des grandes évolutions réglementaires à venir. Réforme européenne, accès aux traitements et transformation digitale étaient au cœur des débats. Un moment riche pour partager et anticiper l’avenir du réglementaire.